CSV胡大侠 - ( 系列文章专栏)CSV法规指南知识库
系列文章专栏)CSV法规指南知识库
CSV胡大侠 -( 博普视频课传送门)
博普视频课传送门)
前言:迎检技巧不是欺骗误导,而是检查中双方更好的配合!
我们应该如何定义所谓的迎检技巧Skill呢?是否说一个企业平时工作做到按质按量,问心无愧,通过检查就是自然而然呢检查员产生“日常GMP管理,也是如此混乱吗”的误解呢
用我之前PIC/S培训导师Joerg Neumann - 领英传送门( 领英传送门)
领英传送门)
“To make it clear right away, it's not about fooling theinspector or inspectors. Any experienced inspector will quickly recognize thisand then there will be no basis for trust. However,Success does depend onhow the inspection is managed.”(首先需要明确的是,迎检技巧并不是来如何愚弄检查员,GMP检查的成功确实依赖于公司面对GMP检查时的应对管理技巧。
当然“打铁还需自身硬”–一个公司良好的GMP日常无法预期的飞行检查
但不可否认的是,飞检现场所有直接因素间接因素被核查公司的有力组织和配合
快速导读 - 工厂飞检迎检技巧知识框架
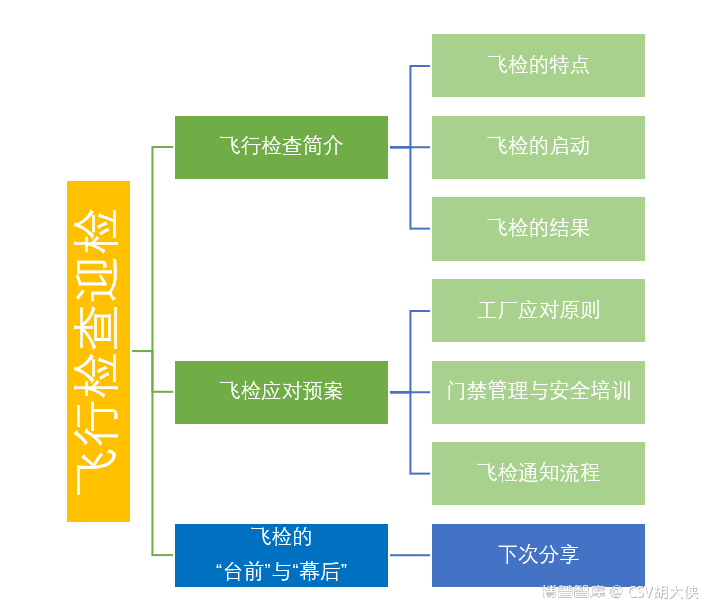
1. 飞行检查法规要求 – 参考2015药品医疗器械飞行检查办法( 药品医疗器械飞行检查办法)
药品医疗器械飞行检查办法)
药品飞行检查药品生产、经营不预先告知【所以最近新闻来看,不仅是药品GMP生产企业,GSP药品分销与终端零售也是飞检的重点!】
1.1 飞行检查的特点
隐秘性:飞行检查安排即使在组织实施部门内也相对隐秘的,只有该项工作的主要领导和具体负责的人员掌握情况,企业所在的药监部门在最后时限才得到通知
突然性:由于飞检的隐秘性,所以,被检查企业事前不可能做任何准备工作,检查组现场所看到的就是企业日常生产管理的真实状况
绝缘性:飞行检查组做到不吃企业的饭,不住企业预订的酒店,不用企业的车,费用由药品认证管理中心和检测员支付;
现场灵活性:药品认证管理中心制定的检查预案,主要确定现场检查要点。检查组现场检查的具体时间及步骤由检查组根据检查需要确定,以确保检测质量
记录即时性:检查员在现场检查过程中,及时填写飞行检查工作记录
独立性:排除一切干扰,只对派出部门负责
专业性:现在国家局组织的飞检,除有飞检经验的检查员外,有时根据需要会指派专业技术人员参加,并对检查人员进行相关知识培训后CS&DI数据可靠性常常是飞检突破口之一广东省人民政府办公厅关于印发广东省推进职业化专业化药品检查员队伍建设实施方案的通知
1.2 飞行检查的启动
参考( 飞行检查方法)
飞行检查方法)
(一)年度监督检查
(二)投诉、举报
(三)检验发现存在质量安全风险的;
(四)药品不良反应/事件监测提示可能存在质量安全风险;
(五)对申报资料真实性有疑问的;
(六)涉嫌严重违反质量管理规范要求;
(七)企业有严重不守信记录的
参考识林《CFDA( CFDA)2015年飞行检查情况,2016年飞行检查趋势分析
CFDA)2015年飞行检查情况,2016年飞行检查趋势分析
有行业人士推测了2016年度的飞行检查趋势 , CFDA会组织大约500次左右的各类检查。飞行检查比例继续增加。 而CFDA检查重点可能包括(节选近2年内被国际官方警告吃了FDA,欧盟警告信的药品价格明显低于平均成本最严格药品管理法 vs 最低集采药品价格药检所评价性药物警戒PV做得不好,在属地之外出现信号聚集现象的市场竞争对手的举报情况最了解你的,不是你自己而是你对手
1.3 飞行检查的结果
参考飞行检查方法( 飞行检查方法)限期整改、发告诫信、约谈;收回或者撤销相关资格认证认定证书暂停生产、销售、使用、进口等召回产品
飞行检查方法)限期整改、发告诫信、约谈;收回或者撤销相关资格认证认定证书暂停生产、销售、使用、进口等召回产品
更多更具体大家也可以去NMPA官网,搜一搜飞检结果通报,后果还是蛮严重的:( https://www.bopuyun.com/admin_article/江苏大红鹰药业有限公司药企因飞检违规,遭到停产处理。)江苏大红鹰药业有限公司药企因飞检违规,遭到停产处理。(
https://www.bopuyun.com/admin_article/江苏大红鹰药业有限公司药企因飞检违规,遭到停产处理。)江苏大红鹰药业有限公司药企因飞检违规,遭到停产处理。( https://mp.weixin.qq.com/s/4T12o8galW4nsfpBpnGXZA)飞检,一药企被立案调查(
https://mp.weixin.qq.com/s/4T12o8galW4nsfpBpnGXZA)飞检,一药企被立案调查( https://mp.weixin.qq.com/s/QpjhBoChDE3izp448kZvMw)2020年医疗器械飞检缺陷汇总
https://mp.weixin.qq.com/s/QpjhBoChDE3izp448kZvMw)2020年医疗器械飞检缺陷汇总
2. 迎检技巧 (上)– 从飞检小组突至到首次会议
2.1 飞检应对原则
u 应严格按照良好生产质量管理规范开展质量管理工作;
u 应建立飞行检查应对预案或管理制度,确保接到通知后5分钟内相关人员就位,并进入迎检状态。
u 对飞行检查应当予以配合,不得拒绝、逃避或者阻碍。
u 应按照检查组要求,明确检查现场负责人,开放相关场所或者区域,配合对相关设施设备的检查,保持正常生产经营状态,提供真实、有效、完整的资料。
2.2 工厂安保原则
一般药企的生产工厂,都需要提前建立好门禁管理及安全培训制度
1. 工厂门禁保确认与接待

2.工厂门禁保安做好来宾信息登记工厂安全负责人交接

3. 工厂安全负责人应要求所有进入工厂人员工厂安全培训安全着装要求(如需,提醒检查员戴头盔,换工衣等)
安全知识与培训时长的平衡考虑不因无故拖延监管老师时间
总而言之,对于工厂应形成日常来访者门禁登记与安全培训制度,并始终严格执行,不因飞检小组而搞特殊,不卑不亢,按制度执行即可。
2.3 飞检通知流程
参考2.2门禁保安登记与通知制度,在飞检老师完成人员登记与安全培训的同时趁这个空档完成飞检关键人员的通知与资料准备
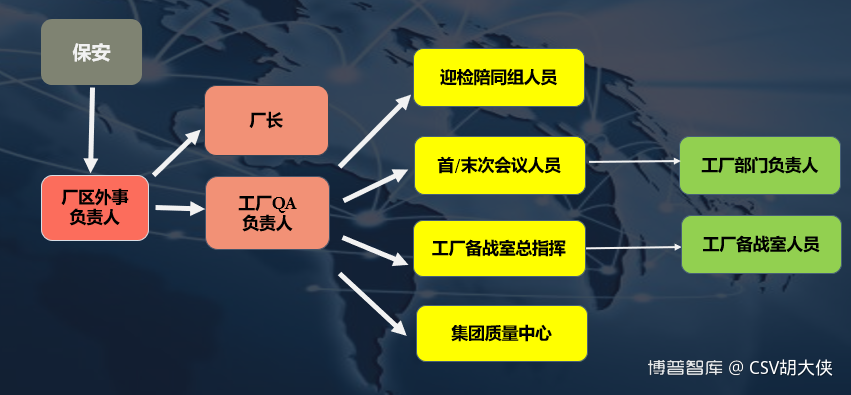
1.提前建立好工厂飞检/迎检微信群适时补充电话通知

提前建立好工厂飞检/迎检小组按照预演

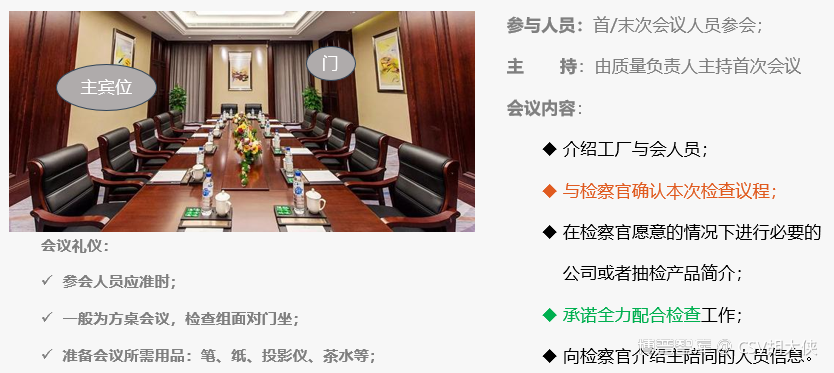
3.等待飞检小组安全培训完成,准备好飞检首次会议的场所与人员,开启首次会议
飞检迎检技巧 - 生产现场检查部分【文章链接
Acknowledge & Reference 特别致谢与引用声明深圳信立泰集团品质中心运营组 冉永梅经理 李敏经理 毕马威中国Life Science 咨询《走向全球经营:中国医药企业的合规挑战( 走向全球经营:中国医药企业的合规挑战)以及以下这位真的为改变中国医药行业,做了不少实事的老毕
走向全球经营:中国医药企业的合规挑战)以及以下这位真的为改变中国医药行业,做了不少实事的老毕

更多阅读
胡大侠 CSV&DI专栏阅读
14.“性能监测/定期审查/再确认&再验证” - 计算机化系统运维方法思考 - 链接
13.药品追溯码/药械UDI信息化追溯体系-《大侠科普Pharm 4.0》系列 2 -链接
12.“审计追踪功能与回顾” - 欧盟GMP期刊翻译与解读 -链接( 链接)
链接)
11.“Data Availability” - ISPE新指南《数据可靠性源于设计》品鉴4- 链接
10.“DCS 与 SCADA相同与不同” - 《大侠科普Pharm 4.0》系列 1 - 链接
9.“Knowledge Management” - ISPE新指南《数据可靠性源于设计》品鉴3 - 链接
8.“Quality Risk Management” - ISPE新指南《数据可靠性源于设计》品鉴2 - 链接
7.“Foundation of DI by Design”-ISPE新指南《数据可靠性源自设计》品鉴1 - 链接( 链接)
链接)
6.《“透明生产即信任!智能制造是未来?” - 参观汤臣倍健智能工厂随笔》- 链接
5.《备份是CSV必要功能吗? - 从电信号/电子数据/电子记录分析real backup data》 -链接
4.《SOP无可操作性&权限控制混乱 - CSV检查的重灾区》 - 链接
3.《老旧生产系统需补做备份还原测试吗?如何做?》-链接
2. 《CSV的OQ&PQ的相同与不同》-链接
1. 《所有计算机化系统都需要定期备份和定期还原测试吗?》-链接

