相关文章推荐阅读
1.问题背景
如文章3( 文章3)所介绍,实施疫苗生产检验记录电子化项目过程中,项目完成顺序是:
文章3)所介绍,实施疫苗生产检验记录电子化项目过程中,项目完成顺序是:
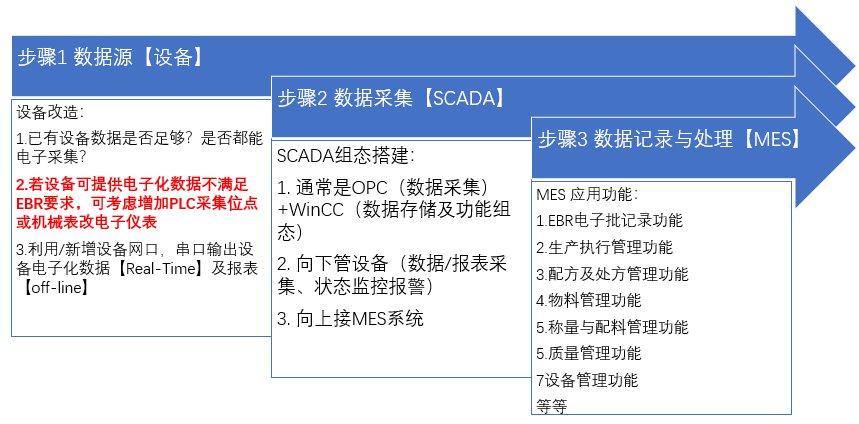
以上图为例,涉及设备改造过程新增位点的过程,有朋友问了一个细节和具体问题是:“关于接入LIMS、MES的设备与仪器的改造变更中,其仪表计量和验证【C&Q 调试与确认】与设备仪器的新机(或改造)确认【Q&V 确认与验证】,是先做仪表计量,还是先做厂家的安装、运行确认呢?”
2.法规指南
2. 1 C&Q 仪器设备的调试与确认
参考药品GMP指南 质量管理体系 3.7.4 确认;试运行(Commissioning)主要依据良好工程管理规范(GEP)执行,是在工程技术方面对厂房、设施、设备等进行的测试和接收,主要关注工程学方面的要求(例如,电路的连接及标识、液压系统等)。
试运行中包括了验收阶段经常涉及到的供应商工厂的验收测试(Factory Acceptance Test, FAT)和用户工厂的验收测试(Site Acceptance Test,SAT),常见的检测项目如下:
2.2 Q&V 仪器设备的确认与验证
中国GMP(98版)第七章“验证”中有如下叙述“第五十七条 药品生产验证应包括厂房、设施及设备安装确认、运行确认、性能确认和产品验证”,其中确认只是作为验证中的一个组成部分存在。而中国GMP(2010版)对验证进行了重新的定义,并将确认作为一个独立的概念从验证中分离出来。其中规定:
3. 先校准 or 先确认?
3.1 法规未明确规定【暂未找到明确条文】
在很多情况下,确认(安装确认和运行确认)是与试运行(包含校准)同时执行的,它们的内容存在重叠的情况,即试运行中的某些测试或检查项目与确认中的项目相类似甚至完全相同(例如,检查并记录设备的型号、功率;与公用系统的连接等)。但确认活动对文件的要求更为严格同时要求质量部门的参与。
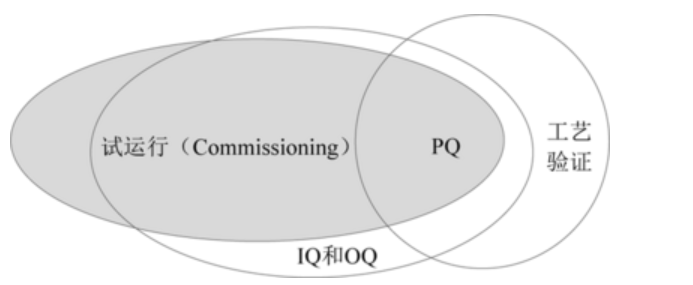
上图引自“ISPE基准指南第五册中‘试运行与确认’”,通过它即可看出试运行、确认以及后续的工艺验证之间的关系。 通常,试运行过程中执行的测试或检查不需要在确认的过程中重复,但是必须保证试运行的文件记录符合GMP的要求,并且过程中有质量部门的参与(如必要的审核和批准)。
3.2 实际经验-看设备仪器特点
1.理想情况是:厂家先完成现场安装及IQ文档,再做计量与调试【C&Q】,最后做功能测试SAT及OQ 文档;
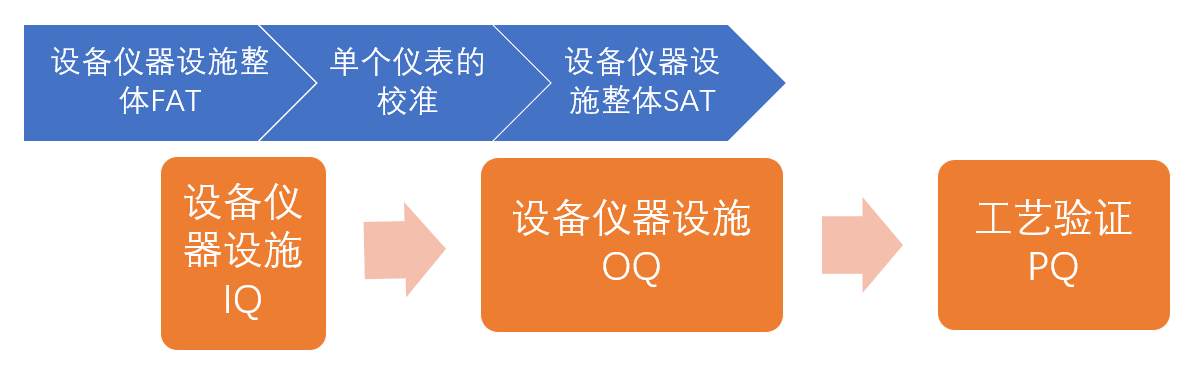
2.实际经验是:分设备仪器的大小,仪表数量,校准送外检或内检
针对于大型的设备,比如灭菌柜,隔离器,纯化设备
它上面会涉及到很多的传感器压差表,压力表等等,那这种时候这些设备上的仪表的校验是可以独立去做的,并不局限于这台设备安装好,这种情况下,你完全可以在安装之前就做完校准。
对于液相这种小型来说,
一般厂家可以先提供安装调试,再过一段时间过来给你做正式的确认;这个中间隔多长时间取决于你自己的要求;但是如果一定要求调试与校准【Commission & Calibration】要在设备IQ与OQ之间,一般还是有点困难的,比如说很简单的设备,厂家要从外地过来想的肯定是一次性做完。,那就需要你很好的去协调计量院的时间了。

