2022年这一年,一直在博普智库平台学习充电,除了和各位智友玩转“智库圈”外,还一直关注“查政策法规”栏目。
在“查政策法规”栏目中可以及时了解相关的“实时快讯”、“最近更新”和“常用政策法规”。
另外,日常还关注了“药械法规”周报和月报。
通过持续不断的学习“药械法规周报”和“药械法规月报”的相关内容,对目前国家的一些动态和监管方向有了一定的了解。
周报和月报中包含了本周或本月的法规相关内容,其中发现周报和月报还是有一定区别的,不是说学习了月报就不关注周报了,因为周报的相关内容会更加的详细,其中里面有作者的相关学习总结和个人看法在里面,而月报则是主要介绍本月法规的整体发布情况,学习部分和作者观点则就没有体现(可能是篇幅的原因),喜欢的朋友可以首页下拉进行关注。
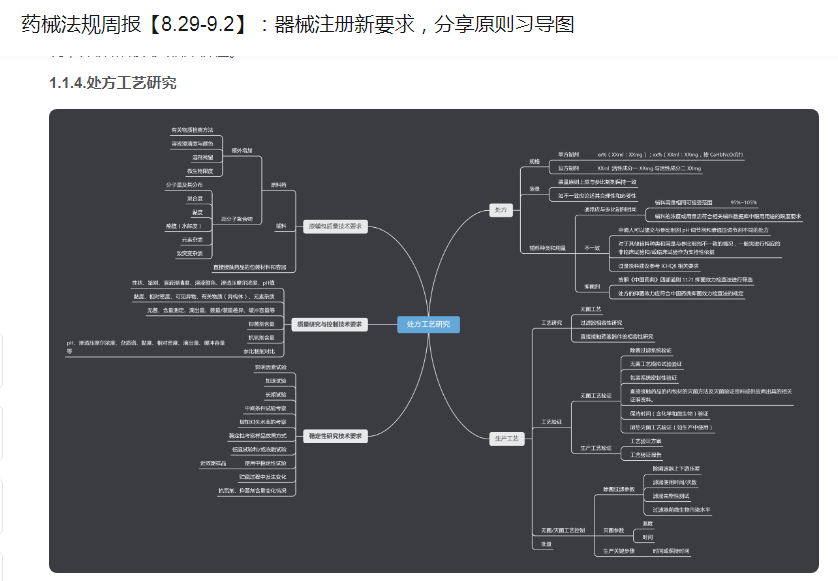
由于与与博普智库平台的管理人员较熟,这不迅速了解到了2022年国家发布的那些指导原则。
截至2022年8月31日,国家发布的文件中与指导原则相关的有76个,其中已实施的指导原则有37个,指导原则征求意见稿(这里的征求意见指单纯的指导原则,不包括指南、工作程序、标准、GMP附录、指导意见、共性问题、检测方法等其他征求意见)有39个。
已实施指导原则文件名称及博普智库相关链接
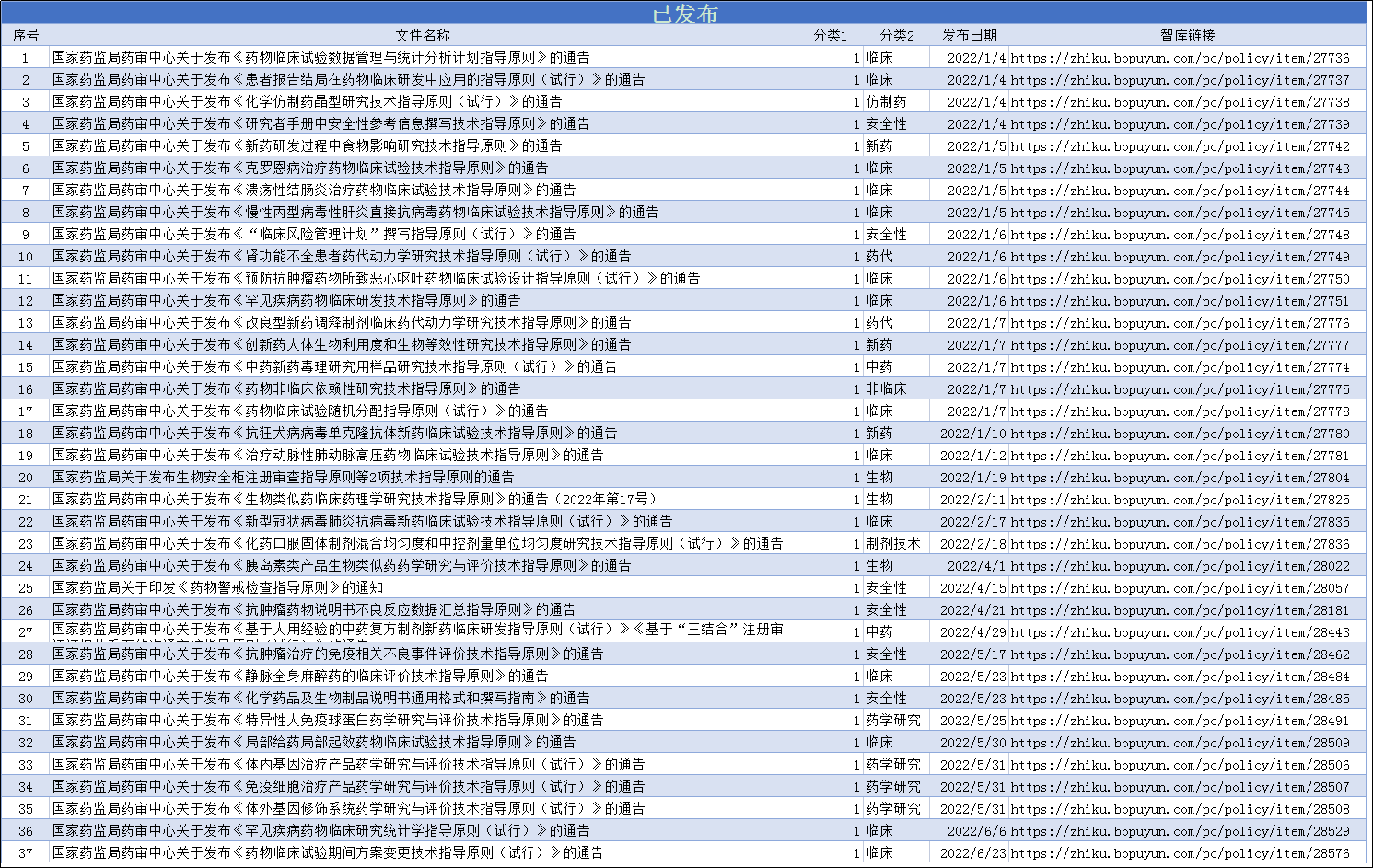
指导原则征求意见文件名称及博普智库相关链接
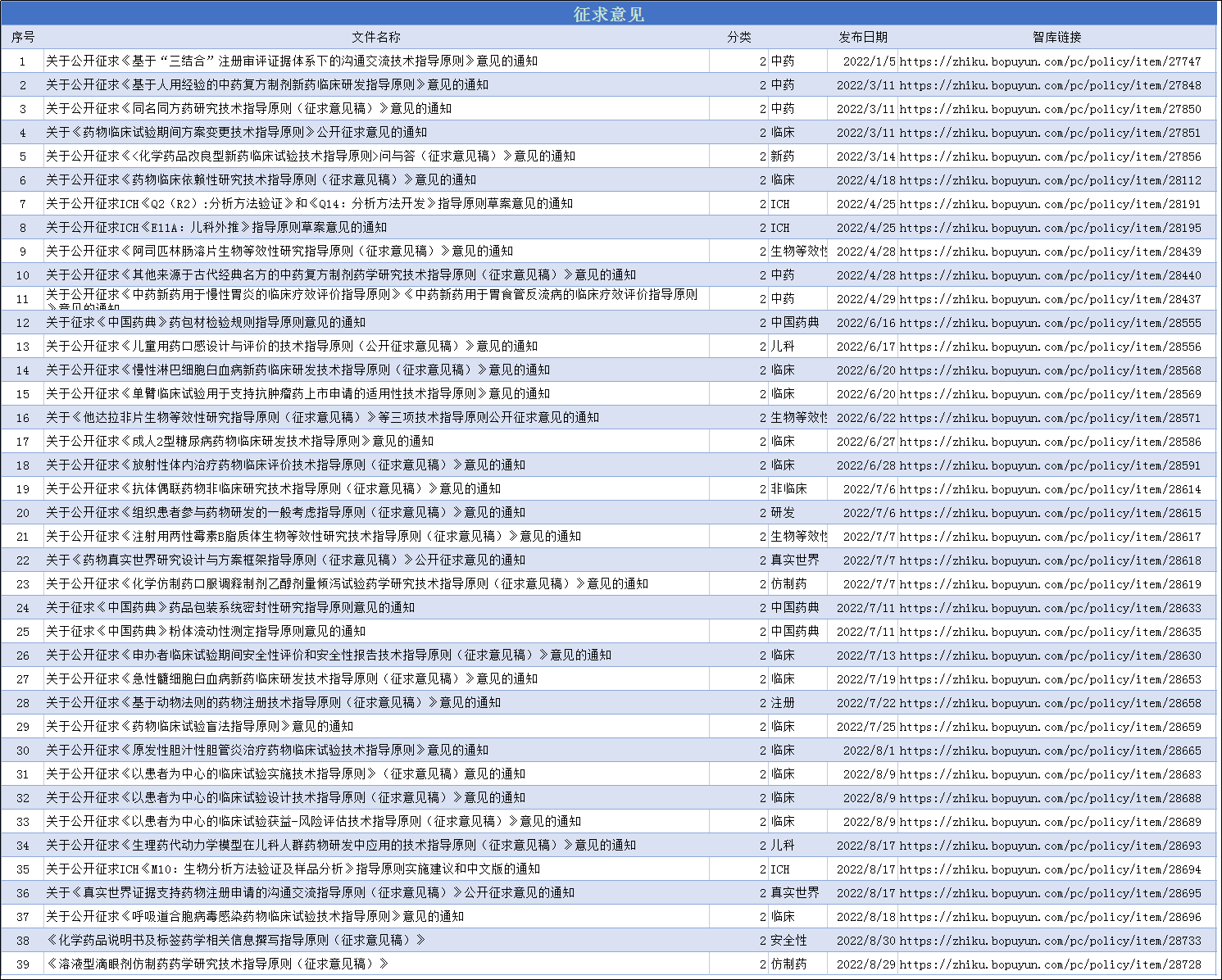
通过时间发布情况来看,已实施指导原则大多数在前半年,征求意见多集中在6、7、8月份。
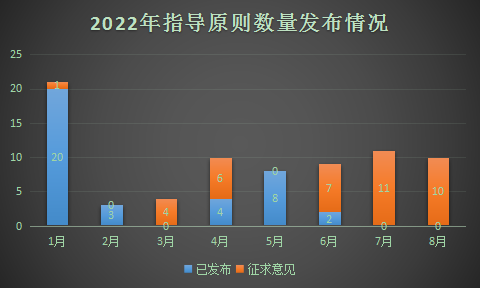
另外根据发布文件相关名称,我还提取了文件中相关的关键词(可能不是很合适,各位智友还望口下留情),来分析相关指导原则发布情况,通过分类情况来看,2022年国家发布的指导原则中涉及的相关内容有临床、非临床、仿制药、儿科、安全性、ICH、注册、中药、中国药典、制剂技术、真实世界、药学研究、药代、研发、新药、生物等效性、生物共计17个方面,其中以临床方面占据最多,这里就需要做临床的小伙伴多多关注国家动向了,以便能够及时了解国家管理动向,从而做好相应工作安排。

2022年,国家发布的指导原则已经有76个,不知道与各位智友相关的又有多少。
但不管是否相关,个人觉得关注一下应该不是一件坏事,毕竟在制药行业,大家也不可能在一家公司、一个方向一直做下去。
随着时间的发展,相信各位智友能够在博普智库得到更多想要的东西,从而充实自己,当机会到来的时候,相信各位智友都能够抓住机会,成为越来越好的自己。

