01前言
制药企业在进行验证活动时,可能会出现测试结果与验证目标不一致的情况。
但对于同一个不一致的情况,也会有不同的产生原因,因而处理方式也不尽相同。
因此应该对不同的偏差进行分类管理,以不同的方法和不同的流程区分对待不同的偏差。这样做一方面能达到降 低质量风险的目的,另一方面也会使得企业的偏差管理体系会更加系统、科学、高效。

根据GMP相关法规和指南的要求,制药企业应当有计划的开展验证活动,从而确保整个生产过程都是受控的。然而在验证过程中不可避免的会出现与验证目标不一致的情况。对于这样的“不一致”需要一套完善的偏差管理体系来支撑,才能达到准确处理与风险控制的效果。
02认识不同偏差
1、验证偏差
验证偏差是由于验证对象本身的不确定因素造成的,因为验证对象未经过确认或验证,不可避免地会出现不符合既定验证目标值的情况。
例如:
贴标机在厂家提供的设备说明书上为300瓶/min,而在验证中只能达到280瓶/min。造成这个偏差的根本原因,是因为厂家在理想状态设定了目标值,而在验证过程中才是真实反应了贴标机的实际能力。

2、常规偏差
常规偏差的原因很多,相比验证偏差更复杂,并且往往需要调查才能找出根本原因。验证过程中发生常规偏差,可能是用于验证的方案不适用导致的。
例如:
使用了错误批号的物料或未被放行的物料,这是人员操作不当导致的常规偏差。
常规偏差的原因可能复杂(多次验证方案不当)也可能简单(单次验证方案不当),但不论是多次还是单次常规偏差都是可以避免的,是可以“不发生”的。
03如何处理不同偏差
1、验证偏差的处理方式
验证偏差是需要记录和解释的,在必要时需要采取相关处理措施。
例如:
通过科学的评估对原先设定的可接受的标准进行调整。再以贴标机为例,当我们在验证过程中发现贴标机只能达到280瓶/min,就应将验证方案中300瓶/min的标准从新定义为280瓶/min。

2、常规偏差的处理方式
常规偏差首先要对其影响性作出初步判断,根据常规偏差对质量的影响进而进行分类。
例如:
归为关键偏差、中小偏差、或是微小偏差。对于微小偏差,如在进行使用前发现仓库发送了错误的物料,这种偏差仅仅需要记录和解释,并及时更换物料修正错误就行了。
但是对于中等偏差和关键偏差,就应当调查其背后的根本原因,再评估偏差造成的影响,并建立纠正和相关预防措施(CAPA),在得到批准后进行相关纠错行动,最后完成相关的偏差报告。
简单来说偏差处理流程如下:
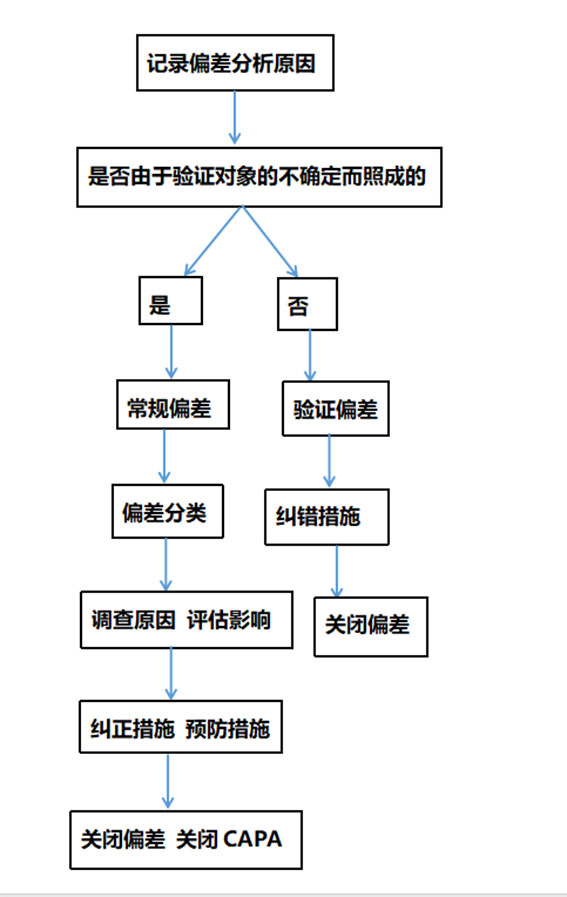
04不同偏差的发生概率也不相同
1、验证偏差
验证偏差对于任何一个全新的验证对象,验证偏差是作为独立事件,只会出现单次,这样的验证偏差是不需要相应的预防措施的。
2、常规偏差
常规偏差是基于某些原因发生了不该出现的偏离,这种偏离是有可能会再次出现的。因而需要在影响评估时分析其发生的可能性,同时需要通过预防措施,降低其发生的可能性,从而降低风险,达到风险控制的目的。

05不同偏差的对比
1、常规偏差
常规偏差如果产生于一个已将合规的系统或设备时,理论上这类偏差是不应该发生的,应评估偏差对人员安全、产品、环境、质量体系等的影响,并基于这些影响进行纠正措施(CA)和预防措施(PA),即需要现场第一时间的纠正和长远的预防。其目的在于减少同类偏差发生的概率,降低质量风险。
2、验证偏差
验证偏差产生于一个未经验证的系统或设备,这类偏差的处理同城只是陈述事实,并且进行纠正,不需要进行预防,目的是如何从偏差状态中恢复,以继续验证实施。
06总结
总得来说在验证过程中出现的偏差一部分属于验证偏差,一部分属于常规偏差。因此药企需要建立完善的偏差管理体系,以区别处理这两类偏差。
这样既能科学、经济的达到验证目的,同时还能降低质量风险、实现将风险控制在可以接受的范围。

