质量风险管理是对风险进行评估、控制、沟通与审查的系统化过程。它是一个重复的流程,贯穿于从概念形成到系统隐退的整个计算机化系统生命周期中。其概述及带来利益如图1。
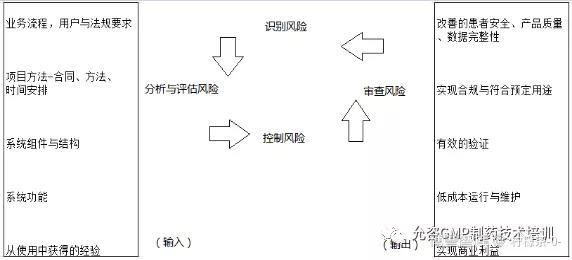
图1风险管理概述及带来利益
目的及益处
计算机化系统的风险管理应用于系统整个生命周期,具体如下图:
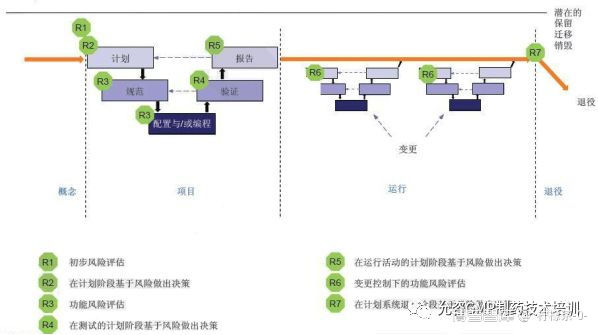
图2应用于计算机化系统整个生命周期的风险管理
计算机化系统的风险主要是针对患者安全、产品质量以及数据可靠性而言的。其目的是:
识别风险并将其消除,或者将其降低到一个可以接受的水平。
针对具体的系统采取适宜的生命周期活动,提供依据和灵活的方法。
它是用一种可控而且合理的方式侧重于计算机化系统的关键方面,其益处主要体现在:
更加关注于患者安全、产品质量和数据可靠性(最终目标),对GxP风险进行有效的识别和管理。
根据系统的整体风险(GxP风险、复杂性和新颖性、供应商评估)确定采用适宜的可增减生命周期活动。
为充分利用供应商的活动(知识、经验和文件)提供依据。
确保系统符合预期用途。
加深对产品和流程的理解。
提高系统合规效率。
更好的识别潜在风险以及建议的控制措施。
其他益处。
质量风险管理流程
计算机化系统质量风险管理采取了同ICHQ9相一致的框架进行风险评估、控制、交流与审查的系统化过程。质量风险评估应基于科学的知识进行,并且最终将与对患者的保护联系起来;质量风险管理流程投入的水平,正式的程度及文件化的深度应与风险的级别相一致,此为质量风险管理的两个原则。如下图展示了GAMP用于质量风险管理的五步流程是如何应用ICHQ9流程来实现和维护系统合规的。
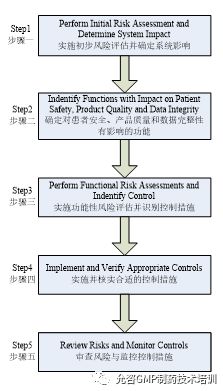

图3ICH Q9流程和GAMP风险管理流程
上述的五步流程将在计算机化系统生命周期的各个阶段所实施。下表展示了每个风险管理步骤下的典型输入和输出。
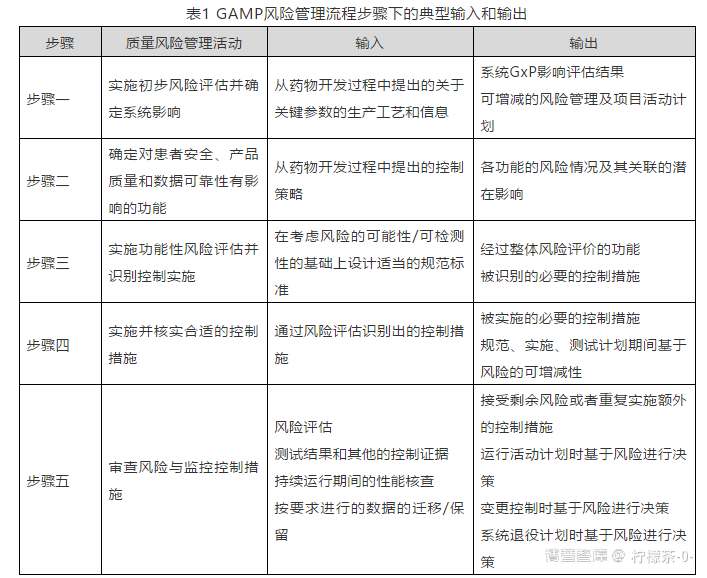
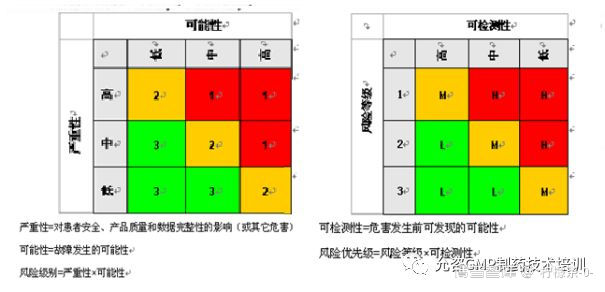
计算机化系统的风险管理工具一般采用如图4所示简化的FMEA模型。
图4简化的FMEA模式
文章来源:允咨GMP制药技术

