1风险分析目的
202X.11.XX~202X.11.XX某某某制药公司接受GMP认证检查,发现《安瓿瓶检漏灭菌柜性能确认方案》(编号123-45-678-00)中对于灌装封口后的安瓿瓶进行灭菌检漏时选择的参数未做详细说明,鉴于此情况在此做出风险评估。
2参考文件
《药品生产质量管理规范》(2010修订)
药品生产验证指南2003年版
药品GMP指南设备设施\无菌药品等
3评估范围
本风险评估报告适用于某某某制药公司注射液车间水针线安瓿瓶灭菌检漏柜性能确认时参数选择。
4风险评估
4.1风险分析评估小组成员
基本上是员工把评估在架子搭起来,各位领导在上面提意见,提意见好提,但评估不好做啊。
4.2 风险识别
4.2.1安瓿瓶灭菌检漏柜功能描述
安瓿瓶灭菌检漏柜主要目的是对灌装封口后的安瓿瓶进行辅助的灭菌和主要的色水检漏功能,以保证能将封口不好的安瓿瓶染色后便于剔除。
4.2.2 安瓿瓶灭菌检漏柜评估
测试项目:对灭菌检漏柜的空载时温度分布、满载时温度分布及色水检漏、最小装载温度分布进行测试。为保证灭菌检漏柜的辅助灭菌效果及色水的检漏功能对相关参数进行评估。温度验证进行最小装载和最大装的验证,保证以后进行产品辅助灭菌过程中装量的范围,色水检漏在满载情况下进行测试,满载情况下能够达到要求,则以后其他的装载量也能达到要求。
4.3风险分析
4.3.1安瓿瓶灭菌检漏柜的测试项目
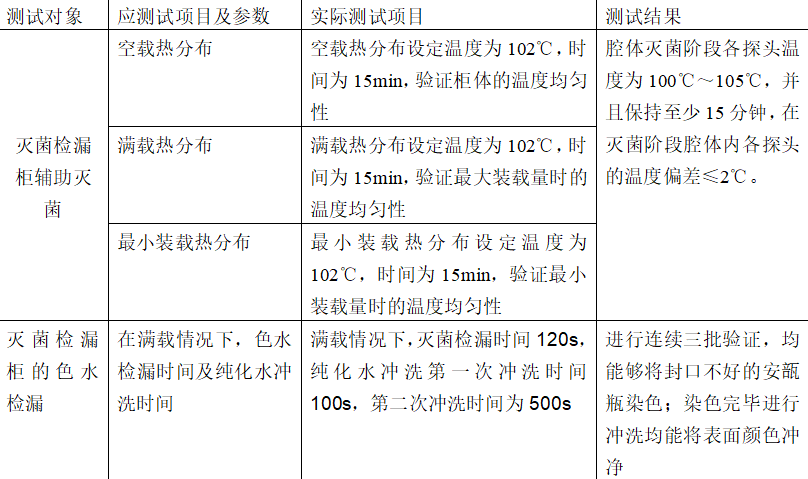
4.3.2 选择测试项目参数的风险分析
根据灭菌检漏柜的参数来评估其GMP关键程度。
关键控制点:灭菌检漏柜的辅助灭菌功能根据不同的品种控制不同的灭菌参数,ABCD注射液的注册工艺中规定灭菌参数(温度控制范围为100℃~105℃,时间15min),灭菌检漏柜的灭菌温度和时间为关键控制参数。色水检漏的效果影响灯检的判断,色水检漏时间(注册工艺120s)为关键控制参数。
非关键控制点:色水检漏后的冲洗时间按照原来的经验值,一次冲洗时间100s,二次冲洗时间500s。冲洗时间短,会出现部分色支,增加灯检的工作量;冲洗时间长浪费能源,增加成本。
a. 灭菌检漏柜的参数选择,验证温度设定为102℃(温度范围在100℃~105℃范围内),时间15min,真空色水检漏的时间120s。参数设定的原因分析:①灭菌检漏柜采用的与原单位一致的设备厂家与型号,ABCD注射液为转移文号的品种,采用与原工艺一致的工艺参数。②ABCD注射液在原厂用“某天”牌设备进行灭菌检漏的参数为温度定为100~105℃,时间15min,色水检漏时间120s,纯化水一次冲洗时间100s,二次冲洗时间500s,灭菌检漏效果良好。基于以上考虑,在灭菌检漏柜性能验证时选择与原工艺参数一致的参数进行验证。
b.灭菌检漏柜验证项目的选择分析:①空载热分布的验证目的是证明柜体本身在温度的均匀性;②满载热分布的选择是按照ABCD注射液在保证能够达到辅助灭菌和色水检漏的前提下的最大装载量进行装载,8盘/层*10层*2车,满载共160盘,验证在满载情况下,温度的分布均匀性及色水检漏的效果。③最小装载热分布的选择是根据实际生产的安排,如果小于半盘的量(即350支)时就废弃,验证在最小装载量时(即350支)的温度分布均匀性。④色水检漏验证选择在满载情况下进行,如果满载情况下色水能够均匀将安瓿瓶染色,那么在其他装载情况下染色也没有问题。基于以上考虑,在灭菌检漏柜性能验证中对于辅助灭菌和检漏的情况进充分验证。
经以上分析,灭菌检漏柜参数的选择合理,验证项目齐全,属低风险。
4.4风险控制
4.4.1 风险控制方法
针对无菌制剂车间水针模块不同级别的风险制定相应的控制措施和合理的纠正预防措施。对于重大风险要消除、预防、降低、转移和检测管理;对于中度风险要降低、管理、控制;对于低风险应采用日常监控或培训等控制手段予以管理。
在现有的条件和控制措施下,无菌制剂车间灭菌检漏柜风险评估得出的风险程度为低风险,不需采取任何控制措施。
4.4.2 风险评估结果落实
当工艺或设备发生了一些变更、大的设备位置变动甚至很重大的变更,要在变更执行完以后就立刻开始风险评估工作。

