高血压是心血管疾病中最常见的风险因素之一。据世界卫生组织(WHO)估计,全球高血压患者人数已达十亿,并且这个数字还在继续上升。
虽然许多患者使用现有的抗高血压药物可以控制血压,但有10~20%的高血压患者仍然无法将血压控制在正常范围内,因此高血压导致的死亡人数仍然排在肿瘤等疾病前面,存在巨大的未被满足的临床需求。
耐药性高血压(Resistant Hypertension,RHTN)是指在应用了≥3种降压药(最大剂量或最大耐受剂量)治疗后血压(BP)仍未得到控制的疾病(BP>140/90~130/80mmHg)。RHTN的主要危害是终末器官损害,包括心力衰竭、中风、缺血性心脏病和肾衰竭,RHTN是全球心血管病过早死亡的主要危险因素。
据德邦证券统计,全球目前共有229个抗高血压上市药物,但还没有专门针对耐药性高血压开发的新药上市。
近日,RHTN新药消息接连发布,一边是Aprocitentan惨遭退货的疑云,另一边是Zilebesiran 2期成功的喜悦,上演了“冰火两重天”的景象。
Aprocitentan遭强生退货
Aprocitentan是一款靶向双重内皮素受体ETA/ETB的口服拮抗剂,内皮素是目前体内较强的缩血管物质,其随高血压分期及舒张分级的病变程度加重而逐级显著升高,特别是在顽固性高血压患者中,此通路经常被发现活化,然而目前并没有抑制此通路的降压疗法。Aprocitentan除了具有抑制内皮素通路的潜力外,且与其他药物产生药物间相互作用的概率低,因而可能成为治疗顽固性高血压患者的新机制药物(此前内皮素抑制剂常用于治疗PAH)。
原本Aprocitentan风头正劲,有望成为近年来首款顽固性高血压药物。
然而,9月6日,Idorsia公司突然宣布从J&J手中“重新取得”共同开发的产品Aprocitentan的全球权利,将支付对方最多不超过3.06亿瑞士法郎(约合3.44亿美元)的对价,包括未来转让处置Aprocitentan所得的30%、转让处置其他产品所得的10%或公司产品销售额的10-15%分成。
图片来源:Idorsia官网
此项决定之所以令人大跌眼镜是因为,Aprocitentan在其三期临床试验PRECISION中表现稳定,并且已经于去年底向FDA递交上市申请,此番操作,不禁令人怀疑是否产品的表现出现了什么颠覆性的结果。
2022年5月,Idorsia宣布,Aprocitentan在治疗顽固性高血压患者的3期临床试验中获得积极顶线结果。Aprocitentan与标准抗高血压疗法联用,在为期48周的疗程中,显著降低患者血压。

图片来源:Idorsia官网
试验共分为三个阶段,第一阶段按1:1:1随机双盲分配到安慰剂组与12.5/25mg的Aprocitentan剂量组,治疗4周;第二阶段所有受试者均转入25mg Aprocitentan,治疗32周;第三阶段重新按1:1随机双盲分配到安慰剂组与25mg的Aprocitentan剂量组,治疗12周。
在第一阶段4周结束时,三个组的收缩压变化分别为-11.5/-15.2/-15.3mmHg,两个剂量组与安慰剂组的收缩压差异分别为-3.8mmHg(p=0.0042)和-3.7mmHg(p=0.0046);在32周的第二阶段,血压持续得到控制;在随后第三阶段的40周结束时,Aprocitentan组与安慰剂组的收缩压差异为-5.8mmHg(p<0.0001)。
整体来看,Aprocitentan对于基线情况很差的顽固性高血压患者,不仅起效较快,在4周内就展现出显著的降压效果,而且在整个48周内都维持有效,安全性也并未出现不能接受的情况,看似完全有希望成为在传统的三联或四联药物基础上的新型降压方案。因此,Aprocitentan从去年发布三期临床结果以来都被寄予厚望,而随着强生的“抛弃”,药物的实际表现究竟如何确实很耐人寻味。
siRNA疗法Zilebesiran再获成功
Zilebesiran是一种RNA干扰药物,它由一个小干扰RNA(siRNA)与N-乙酰半乳糖胺(GalNac)配体共价链接组成,可特异性减少肝血管紧张素原mRNA水平,从而减少血管紧张素原水平。
今年7月,Zilebesiran治疗高血压的Ⅰ期研究结果在NEJM杂志上发表。结果显示,zilebesiran单剂给药后,血清血管紧张素原水平和24小时动态血压出现剂量依赖性下降,并且可持续长达24周(6个月)。研究中观察到轻度注射部位反应,无关于低血压、高钾血症或需要药物治疗的肾功能恶化的报道。
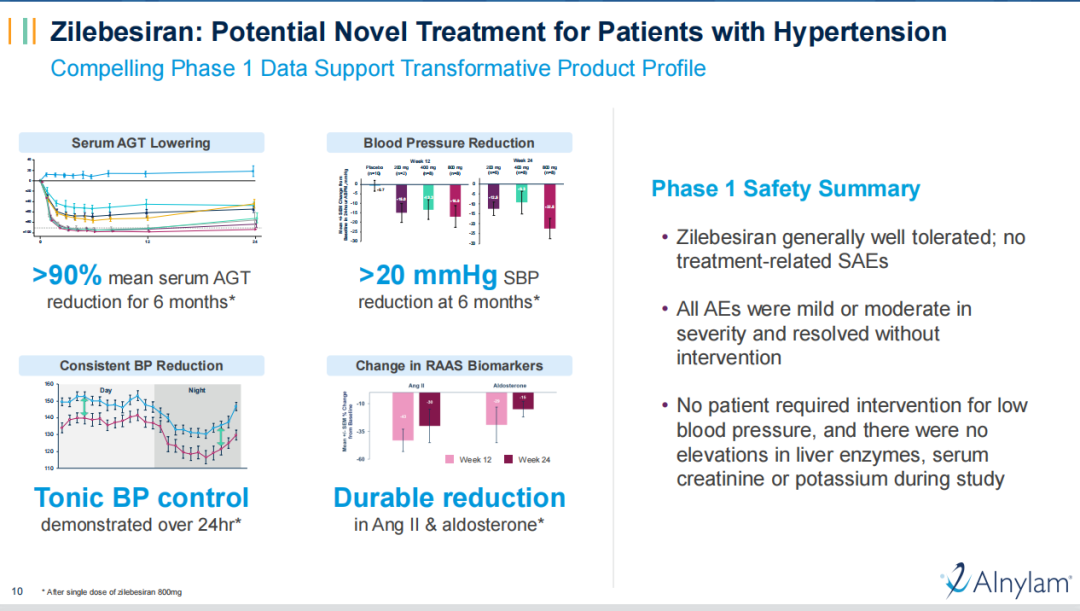
图片来源:Alnylam
几日后,Alnylam宣布与罗氏公司达成战略协议,共同开发和商业化Zilebesiran。根据协议,罗氏将支付3.1亿美元预付款,以及里程碑金额和销售分成,总金额最高可达28亿美元。
9月7日,罗氏和Alnylam公布了Zilebesiran治疗高血压的2期临床试验KARDIA-1数据。公告指出,治疗3个月时24小时平均收缩压(SBP)呈剂量依赖性的显著下降,300mg、600mg剂量组相比安慰剂组降低幅度都超过15mmHg,达到了KARDIA-1 试验的主要终点。
在安全性方面,有1位接受Zilebesiran治疗的患者发生心肺骤停而死亡,但经调查显示,以上死亡事件及不良反应发生均与Zilebesiran的应用无任何关联。另外在Zilebesiran组和安慰剂组的严重不良事件发生率分别为3.6%、6.7%。
目前的研究结果显示,Zilebesiran有可能通过每季度或每半年给药一次的方式实现持续降压。
除KARDIA-1外,Zilebesiran还在进行另一项规模更大的2期研究,用于与标准治疗降压药物联合用药(KARDIA-2)。该研究已于今年 6 月结束,预计将于 2024 年初获得初步结果。
小 结
耐药性高血压是典型的未满足临床需求,至今仍没有可靠的药物治疗方案,但已有不少企业瞄准这一赛道。
据德邦证券统计,RHTN在研新药包括4大新机制+2种新Modality。
四种新机制:
非甾体盐皮质激素拮抗剂,较螺内酯副作用大幅降低,适合长期使用。
氨肽酶A抑制剂,作用于大脑。
双重内皮素拮抗剂,首次在肺动脉高血压基础上的突破。
没有糖皮质激素活性的醛固酮合成酶抑制剂。
两种新Modality:
siRNA,可半年注射一次,解决依从性不好带来的耐药性问题。
ASO,每周一次给药。
除了上文提到的Aprocitentan和Zilebesiran,醛固酮合成酶抑制剂(ASI)Baxdrostat也备受关注。但在今年美国心脏病学会(ACC)年会暨世界心脏病学大会(WCC)上,Cincor公布的2期临床试验(HALO)显示,未达到主要终点,即,与安慰剂相比,Baxdrostat组的平均坐位 SBP 相对于基线无统计学显着变化。但HALO的首席研究仍然对这种新型降压药持乐观态度,Baxdrostat仍将进入3期研究,期待Baxdrostat的最终表现。
IONIS公司开发的靶向AGT的ASO疗法IONIS-AGT-LRx是另一种高血压小核酸疗法,作用机制与Alnylam的Zilebesiran同理:通过降低AGT的表达,从而抑制RAAS通路来降低血压。但该药注射周期为每周一针,在用药便捷性方面远不如半年一次的Zilebesiran。
当然,国内药企也不会错过这一潜力市场。
亨利医药开发的新一代非甾体类选择性盐皮质激素受体拮抗剂(MRA)——Ocedurenone(KBP-5074)用于中晚期慢性肾脏病合并未控制高血压的CLARION-CKD 3期临床试验正在全球同步展开。
信立泰的1类新药SAL0120片已获批临床,用于治疗轻、中度原发性高血压。
瑞博生物9月初公布了其靶向肝血管紧张素原(AGT)的GalNAc-siRNA R0797070临床前研究数据,该候选药物可高效抑制肝脏AGT表达,持续降低血压,显著改善左心室肥厚。
期待新机制的高血压药物的诞生,以造福全球更多患者。
Reference:
1. https://www.nejm.org/doi/full/10.1056/nejmoa2213169
2. https://www.tctmd.com/news/halo-baxdrostat-no-better-placebo-uncontrolled-hypertension
3. https://www.ajmc.com/view/halo-misses-end-point-but-optimism-remains-for-baxdrostat-in-resistant-hypertension
4. https://www.nejm.org/doi/pdf/10.1056/NEJMoa2208391
5. 德邦证券:耐药性高血压市场空间过百亿,新药研发捷报频传

责任编辑:琉璃
声明:本文观点仅代表作者本人,不代表药智网立场,欢迎在留言区交流补充;如需转载,请务必注明文章作者和来源。如涉及作品内容、版权和其它问题,请在本平台留言,我们将在第一时间处理。
声明:本文内容由平台创作者发布,内容仅代表作者本人观点;如内容涉及违法、侵权等情形,请及时联系工作人员处理!工作人员微信:pckt6842。



